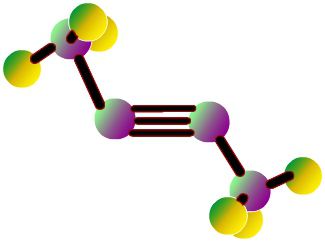
Structuurformule is een grafische weergave van een stof
Sinds de oudheid is de samenstelling van elke stof geaccepteerd in de chemieregistreren in verkorte vorm, met behulp van symbolen en indices (cijfers). Het record in deze vorm wordt de "empirische" formule genoemd. Dus, bijvoorbeeld, de samenstelling van fosforzuur wordt weerspiegeld in deze vorm - H3PO4. Uit dit verslag volgt dat het fosformolecuulzuur bestaat uit drie waterstofatomen, één - fosfor en vier - zuurstof. Het is echter niet duidelijk hoe de elementen met elkaar verbonden zijn, d.w.z. E. informatie is onvolledig. Om deze kloof te overbruggen, wordt de structuurformule van de stof gebruikt.

Zo'n verbindingsrecord heeft een groteinformatief, omdat Met behulp hiervan wordt schematisch getoond hoe en in welke volgorde de elementen van materie met elkaar zijn verbonden. In dit geval wordt elke covalente binding (een paar elektronen) weergegeven door een streepje en komt overeen met één valentie-eenheid.
Zo heeft zuurstof bijvoorbeeld een valentie van tweeomringd door twee streepjes, waterstof - valentie één, daarom één streepje, fosfor - vijf, vijf streepjes. Op basis van dit schrijven kunnen we de chemische eigenschappen van stoffen aannemen, classificeren en systematiseren.
Structuurformule kan in volledige en verkorte vorm worden geschreven. Wanneer het record wordt uitgevouwen, worden alle verbindingen tussen atomen aangegeven en wanneer geschreven in verkorte vorm - nr.
Het meest zichtbaar en significant is hetgrafische voorstelling van de verbindingen in de organische chemie. Immers, de eigenschappen van stoffen niet alleen afhankelijk van het aantal atomen en moleculen, maar ook de volgorde van hun verbindingen. Dit verschijnsel wordt "isomeren" (vertakking van de koolstofketen).
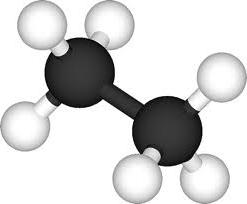

De structuurformule van de stof geeft ook aanfunctionele groepen van koolhydraten: alkylgroep - in alcoholen, aldehyde - in aldehyden, benzeenkern - in aromatische verbindingen. Bovendien is het met behulp van een schematische afbeelding gemakkelijk om de aanwezigheid van karakteristieke bindingen van beperkende koolwaterstoffen te "zien" - een enkele covalente binding. Onverzadigd: ethyleen - een dubbele binding, dieen - twee dubbele bindingen, triple - acetyleen.
De structuurformule van fructose is een voorbeeldruimtelijke isomerie. Dit koolhydraat heeft dezelfde kwantitatieve en kwalitatieve samenstelling als glucose. In oplossingen komt in één keer in verschillende vormen. Uit de grafische formule van fructose kan worden afgeleid dat het keton- en hydroxylgroepen bevat, d.w.z. deze stof heeft de "dubbele" eigenschappen van alcoholen en ketonen. Deze formule maakt het ook mogelijk vast te stellen dat deze keton-alcohol wordt gevormd door de residuen van cyclische a-glucose en pentose (fructose).
De structuurformule is dus een grafische weergave van een stof waarmee men kan leren over de rangschikking van atomen in een molecuul, rekening houdend met het type binding en hun kenmerken.